세라믹 DSC TGA TMA STA 세타람 열분석보고서 | CERAMIC DSC TGA TMA
- 세라믹 (CERAMIC) 소재의 열적 특성을 분석한 DSC TGA STA TMA(열기계물성) 측정 보고서와 해당 모델 소개 사이트 입니다.
- 스위스 KEP Technologies 그룹의, 세타람 브랜드 제품 입니다.
세라믹 열분석이 필요한 이유 ?
Ceramic DSC, Ceramic TGA, Ceramic TMA로 무엇을 분석하나 ?
세라믹 소재 특성과 열적 거동의 관계 :
- 세라믹은 산소 조성, 결정상, 미세구조에 따라 물성이 크게 변함
- 고온 공정(소결, 열처리, 사용 환경)에서 열적 안정성 평가 필수
연구 제조 현장에서의 주요 분석 과제 :
- 상전이 온도 및 상평형(Phase Diagram)
- 산소 비율(Oxygen Ratio) 및 화학양론(Stoichiometry)
- 소결 수축 거동(Sintering Behavior)
- 열팽창계수(CTE), 비열(Cp) 등 열물성
- 생성 엔탈피 및 반응성(Heat of Formation)
세라믹 분석에 사용되는 열분석 기법 개요
Ceramic DSC / Ceramic DTA : 상전이 및 반응 엔탈피 분석 :
- 결정상 전이, 용융, 재결정화 등의 특성 온도 측정
- 고온 영역에서는 Tri-couple DTA 센서로 감도 향상 가능
Ceramic TGA : 산소 조성 및 질량 변화 분석 :
- 산화 환원 반응에 따른 질량 변화 기반 산소 화학양론 평가
- 고체 전해질, 혼합 이온전도체 세라믹 분석에 활용
Ceramic STA : 질량 변화와 열효과의 동시 분석 :
- TGA + DSC/DTA를 하나의 실험에서 동시 수행
- 상전이 + 산화 환원 거동을 연계 해석 가능
Ceramic TMA : 소결 거동 및 열팽창 분석 :
- 소결 중 수축 팽창 거동 실시간 측정
- 분말 소결, 3D 프린팅 세라믹의 공정 조건 최적화
칼베 열량계(Calvet, Drop Calorimetry) : 생성엔탈피 측정
- 고온에서의 열용량, 상전이 엔탈피, 생성엔탈피 정밀 측정
- 열역학 데이터 기반 반응성 예측 및 상평형 계산에 활용
세라믹 주요 응용 분석 항목
상평형 및 고온 상전이 분석 :
- ZrO₂(이산화지르코늄), Y₂O₃(산화이트륨) 등 2000 °C 이상 초고온 상전이 측정
- 냉각 곡선 기반 상전이 신호의 재현성 확보
산소 비율 및 비화학양론 분석 :
- LaGaO₃계 (란타넘 갈륨 산화물계), LSGM(란타넘 스론튬 마그네슘 갈륨 산화물) 계열 세라믹의 산소 결손량(δ) 계산. 고체 산화물 연료전지(SOFC)의 핵심 부품인 전해질로 사용되는 페로브스카이트 구조의 세라믹 입니다.
- 환원 산화 분위기 전환 실험 가능
소결 수축률 및 공정 제어 :
- 소결 중 수축 속도 제어를 통한 최종 치수 안정성 확보
- 산업용 소결로 조건 설정을 위한 기준 데이터 확보
열팽창계수(CTE) 및 열물성 평가 :
- 구조물 내 열응력 및 파손 가능성 예측
- 접합 복합 구조 설계 시 핵심 물성 데이터
비열(Cp) 및 고온 열안정성 :
- 제조 공정 및 사용 환경에서의 열노화 안정성 평가
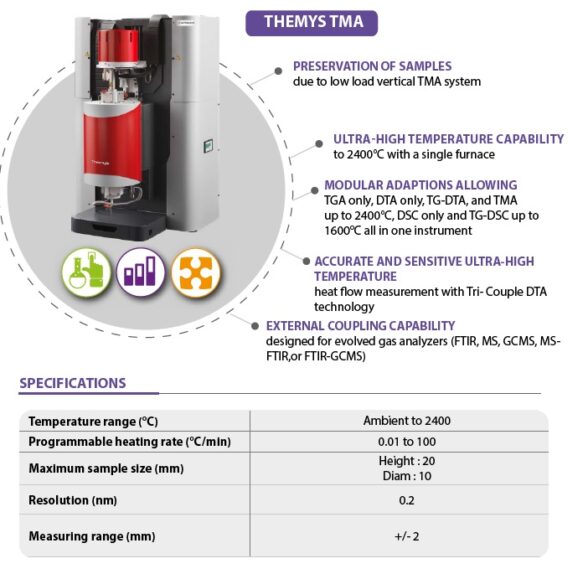
세라믹 연구를 위한 세타람 열분석 시스템의 특징
초고온 단일 퍼니스 설계
- 최대 1600 – 2400 °C 단일 퍼니스 운용
- 고온 실험 시 온도 재현성 확보
모듈형 플랫폼 구성
- TGA / DSC / DTA / STA / TMA 하나의 시스템에서 확장 가
- 연구 단계 변화에 따른 유연한 구성
가스 분석기 연동(EGA)
- FT-IR, MS, GC-MS 등과 연동하여 방출 가스 동시 분석
장비 모델별 상세 소개
- THEMYS STA / TMA / TGA
- THEMYS ONE
- 모델 CALVET 열량계 (Drop Calorimetry)
세라믹 실험 보고서 적용 사례
- 상전이 분석 사례
- 소결 및 열팽창 실험
- 산소 화학양론 및 생성엔탈피 측정
본 페이지의 아래 열분석 측정 사례는
- SETARAM의 일반 버전 모델 SETLINE DSC, 모델 SETLINE TGA 및
- 상위버전 초미세 DSC인 모델 CALVET 시리즈
- 상위버전 TGA, STA
열량 분석 장비를 기반으로한 실제 실험 보고서와 데이터 입니다.
2000~2400°C 범위에서 세라믹 소재인 이트리아와 지르코니아의 상전이 특성 분석 :
모델 THEMYS에서 – STA 기능 사용

소개
- 고온 차등 열분석(High-temperature Differential Thermal Analysis, DTA)을 이용하여 지르코니아(ZrO₂)와 이트리아(Y₂O₃)의 고온 가열후 냉각시험 과정에서 상전이(phase transition)에 대한 데이터를 얻었다.
- ZrO₂의 정방정계(tetragonal) 구조는 2,311 ± 15 °C에서 입방정계 플루오라이트(Cubic fluorite) 구조로 전이하며, 이때 엔탈피 변화는 3.4 ± 2 kJ/mol이다.
- C-type 입방정계 Y₂O₃는 2308 ± 15 °C에서 상전이가 발생하며, 이 상전이는 플루오라이트 구조로의 전이일 가능성이 높다. 이때의 엔탈피 변화는 ΔH = 47.7 ± 3.0 kJ/mol이다.
- 이 고온 다형체(high-temperature polymorph)는 2,382 ± 15 °C에서 용융되며,
- 융해 엔탈피(enthalpy of fusion)는 35.6 ± 3.0 kJ/mol로 측정되었다.
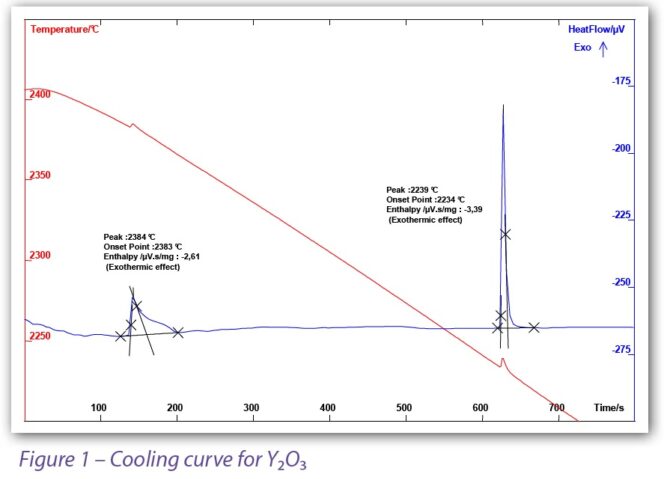
- X축 (Time/sec) : 실험이 진행되는 시간(초)을 나타냅니다. 시간의 흐름에 따라 시료가 냉각되면서 발생하는 열 변화를 기록한 것입니다.
- 좌측 Y축 빨강색 곡선 (Temperature, °C) : 프로그램된 온도 변화 또는 실제 시료 온도를 나타냅니다. 붉은색 곡선은 시간에 따라 감소하는 냉각 온도 프로파일을 의미합니다.
- 우측 Y축 파랑색 곡선 (Heat Flow, µV) : 시료에서 발생하는 열 유속(Heat Flow) 신호를 나타냅니다. 파란색 곡선은 시료에서 발생하는 열 효과(발열 또는 흡열 반응)를 보여줍니다.
실험 방법
- 실험에는 텅스텐(Tungsten) 도가니가 사용되었다.
- 각 실험 전에 온도 및 감도 보정(calibration)을 수행하였다.
보정은 텅스텐 도가니 내에서 α-알루미나(alpha-Al₂O₃)의 용융 실험을 수행하여 이루어졌으며, 조건은 다음과 같다.
- 가열 속도: 10 °C/min
- 분위기: 헬륨(He)
- α-알루미나 용융 온도: 2052 °C
- 융해 엔탈피: 1092 J/g
지르코니아 분석의 경우 실험 종료 후에도 추가 보정을 수행하였다.
그 결과 온도 보정값이 약 50 °C 증가한 것으로 관찰되었다.
이 변화는 주로 2400 °C 고온 가열 과정에서 열전대(thermocouple)의 열화(aging)에 의해 발생한 것으로 판단된다. 각 시료는 다음과 같은 조건으로 분석되었다.
가열 과정 (Heating run) 후 냉각 하면서 측정
- 온도 범위: 1600 °C → 2400 °C
- 가열 속도: 10 °C/min
이후 스캔 방향을 반대로 하여 냉각 과정(cooling run)을 수행하였다.
결과 및 결론
일반적으로 냉각 과정(cooling run)에서 얻은 신호가 초기 가열 과정보다 더 명확하게 나타났다.
이는 시료가 한 번 가열된 후 도가니(pan)와의 열접촉이 개선되기 때문으로 판단된다.
예로서 Figure 1은 이트리아(Y₂O₃)의 냉각 곡선을 보여준다.
지르코니아의 경우 t 정방정계 → c 입방정계 상전이가 명확하게 관찰되었으며, 세 번의 실험에서 다음과 같은 피크 온도가 측정되었다.
- 2265 °C
- 2278 °C
- 2311 °C
ZrO₂ 및 Y₂O₃ 상전이에 대한 권장 열역학 파라미터
본 연구 결과는 지르코니아(ZrO₂)와 이트리아(Y₂O₃)의 상전이에 대한 열역학적 파라미터의 기준값(recommended values)을 제시한다.
| Material | Transition | T (°C) | ΔH (kJ/mol) | ΔS (J/mol/K) |
|---|---|---|---|---|
| ZrO₂ | m → t | 1199 | 5.43 ± 0.31 | 3.69 ± 0.21 |
| ZrO₂ | t → c | 2311 | 3.4 ± 2.1 | 1.3 ± 0.8 |
| Y₂O₃ | c → c | 2308 | 47.7 ± 3.0 | 18.5 ± 1.2 |
| Y₂O₃ | c → m | 2382 | 35.6 ± 3.2 | 13.9 ± 1.2 |
- m = monoclinic (단사정계, 가장 비대칭 구조), t = tetragonal (정방정계, 축하나만 길이 다름), c = cubic (입방정계, 가장 대칭적 구조) → 모두 고체 상태에서 발생하는 결정 구조 상전이. 결합 자체는 유지 되고, 원자배열 구조만 달라짐, 결정격자만 재배열.
- ZrO₂에서 m, t, c 는 온도에 따라 안정성이 달라지며, 저온에서는 m 구조가 안정하고 온도가 상승할수록 t, c 구조가 안정해진다.
- sharp peak (흡열 또는 발열 피크) 특정 온도에서 발생
예를 들어 ZrO₂
- 약 1199°C → monoclinic → tetragonal
- 약 2311°C → tetragonal → cubic
- 약 2700°C 이상 → 그 이후에야 용융(liquid)
- 즉 m-t-c 전이는 모두 고체 상태에서 발생합니다.
세라믹에서 중요한 이유
특히 ZrO₂에서는
m → t 전이 시 약 4~5% 부피 변화, 그래서
- 세라믹 균열
- transformation toughening
- 소결 거동
에 매우 중요합니다.
참고문헌 (Reference)
Navrotsky, A., Benoist, L., Lefebvre, H.
이트리아(Y₂O₃)와 지르코니아(ZrO₂)의 2000°C–2400°C 구간 상전이 엔탈피의 직접 열량 측정
Journal of the American Ceramic Society (미국 세라믹 학회지),
Vol. 88, No. 10, pp. 2942–2944, 2005.
지르코니아의 고체 상전이 :
모델 THEMYS – STA 기능 사용

소개
- 상전이(Phase transition)는 일반적으로 DTA(Differential Thermal Analysis, 시차 열분석) 또는 DSC(Differential Scanning Calorimetry, 시차주사열량계) 센서를 사용하여 분석된다.
- 이러한 기술은 저온 영역에서는 매우 높은 감도를 가지지만, 1,000°C 이상 고온 영역에서는 일부 한계가 나타날 수 있다.
- SETARAM의 THEMYS 열분석기(Thermal Analyzer)는 이러한 문제에 대해 TRI-COUPLES DTA 센서라는 흥미로운 대안을 제공한다.
- 이 센서는 일반적인 DTA 센서가 각 도가니(crucible) 아래에 1개의 열전대 접점(thermocouple junction)을 사용하는 것과 달리,
- 각 도가니 아래에 3개의 열전대 접점을 배치하도록 설계되어 있다.
- 또한 DSC 센서보다 사용되는 재료량이 적기 때문에, 고온에서 발생하는 *기생 복사열(parasitic radiative effects)*의 영향을 덜 받는다.
- 이러한 설계는 수집되는 열량(heat collection)과 센서 감도(sensitivity)를 크게 향상시킨다.
- 따라서 고온 영역에서 발생하는 낮은 에너지 수준의 열 현상(low energy phenomena)도 이 센서를 사용하면 정확하게 측정할 수 있다.
- 예를 들어 약 1,200°C에서 발생하는 지르코니아(ZrO₂)의 고체-고체 상전이 (단사정계 → 정방정계, Monoclinic → Tetragonal)가 시험되었으며, 그 결과는 표준 DSC 센서와 비교 되었다.
실험 방법
다음과 같은 실험 절차가 사용되었다.
- 시료 (Sample) : 지르코니아 분말 (Zirconia powder)
- 질량 (Mass) : DTA : 83 mg DSC : 87 mg
- 기준 시료 (Reference) : 빈 Al₂O₃ 도가니
- 가열 조건 (Heating) : 800 – 1500°C, 가열 속도 10 K/min
- 장비 (Apparatus) : 모델 THEMYS 열분석기 + Type S TRI-COUPLE DTA 센서 또는 DSC 센서
- 분위기 (Atmosphere) : 공기 20 ml/min
Figure 1 : 위 쪽에 측정 그래프 있습니다.
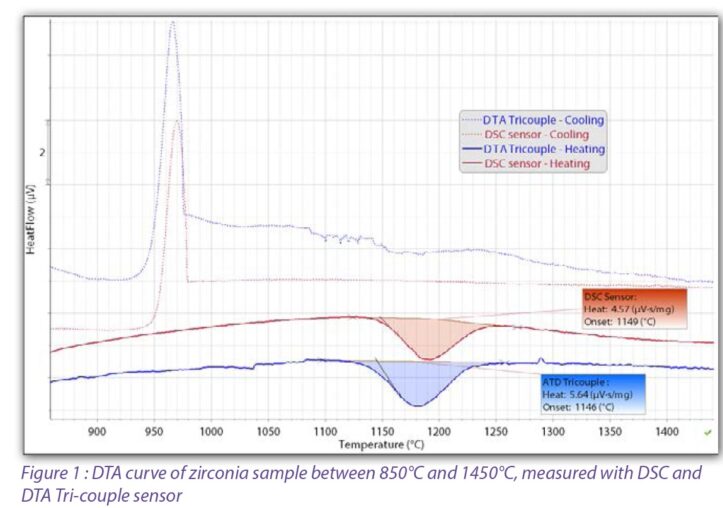
850°C ~ 1450°C 범위에서 측정된 지르코니아 시료의 DTA 곡선
DSC 센서 VS DTA TRI-COUPLE 센서 비교
→ 분홍색 선이 DSC 곡선, 파랑색 선이 DTA Tri-Coupled 센서 측정)
위 그래프는 850°C ~ 1450°C 구간에서 지르코니아(ZrO₂) 시료를 분석한 DTA/DSC 곡선을 보여줍니다.
약 1150°C 부근에서 흡열 피크(endothermic peak)가 나타나며, 이는 단사정계(monoclinic) → 정방정계(tetragonal) 상전이에 해당 합니다.
가열 과정에서 측정된 열량은 다음과 같습니다.
- DSC 센서 : Heat ≈ 4.5 µV·s/mg, Onset ≈ 1181°C
- DTA TRI-Couple 센서 : Heat ≈ 5.4 µV·s/mg, Onset ≈ 1176°C
측정 결과 DTA TRI-Couple 센서가 DSC 센서보다 약 23% 높은 열 신호(감도)를 나타내어 고온에서 발생하는 작은 열 변화를 더욱 선명하게 검출할 수 있음을 확인할 수 있습니다.
냉각 과정에서는 정방정계 → 단사정계로의 역상전이(recrystallization)가 나타나며,
가열 시보다 더 낮은 온도에서 피크가 발생하고 신호가 더욱 뚜렷하게 관찰 됩니다. 이는 가열 후 시료와 도가니 사이의 열접촉이 개선되기 때문입니다.
결과 및 결론
- 가열 과정에서 1125°C ~ 1225°C 구간에서 흡열 반응(endothermic effect)이 측정되었다.
- 이 반응은 지르코니아의 단사정계(monoclinic) → 정방정계(tetragonal) 고체 상전이에 해당한다.
- 이 현상은 DTA TRI-COUPLE 센서와 DSC 센서 모두에서 관찰되었지만,
- DTA TRI-COUPLE 센서의 감도가 약 23% 더 높게 나타났다.
- 따라서 이 센서 구조는 고온에서 발생하는 열 현상을 더욱 정밀하게 측정할 수 있게 한다.
- 또한 냉각 과정에서는 더 낮은 온도에서 단사정계(monoclinic) 구조로의 재결정(recrystallization)도 관찰되었다.
수축률 제어를 통한 Al₂O₃ 소결 :
모델 THEMYS – TMA 기능 사용
소개
세라믹 소재는 소결(sintering) 과정에서 치수가 크게 변화하기 때문에,
최종 제품이 요구되는 치수와 물성을 갖도록 이러한 변화를 제어하는 것이 매우 중요하다.
TMA (Thermomechanical Analysis, 열 기계물성 분석)는 다음과 같은 정보를 제공한다.
- 소결 과정에서의 체적 수축(volume shrinkage)
- 분말 입자 성장(powder grain growth)
- 이러한 현상들 간의 상호작용
모델 THEMYS TMA는 실험 중 소결 속도(sintering rate)를 제어할 수 있는 기능을 제공하며,
이를 통해 산업용 소결로(industrial sintering furnace)에 적용할 최적의 온도 프로파일에 대한 중요한 정보를 얻을 수 있다.
실험 방법
직경 10 mm, 높이 20 mm의 원통형 알루미나(Al₂O₃) 시료를 사용하였다.
실험 조건은 다음과 같다.
- 가열 속도 : 5 K/min
- 최대 온도 : 1780°C
- 프로브(probe) : 알루미나 프로브
- 캐리어 가스 : 헬륨(He)
소결 속도 제어 조건
- 최대 수축 속도(Maximum shrinking rate) : 20 μm/min
- 수축 속도 제어 : 전용 소프트웨어 패키지를 사용하여 제어
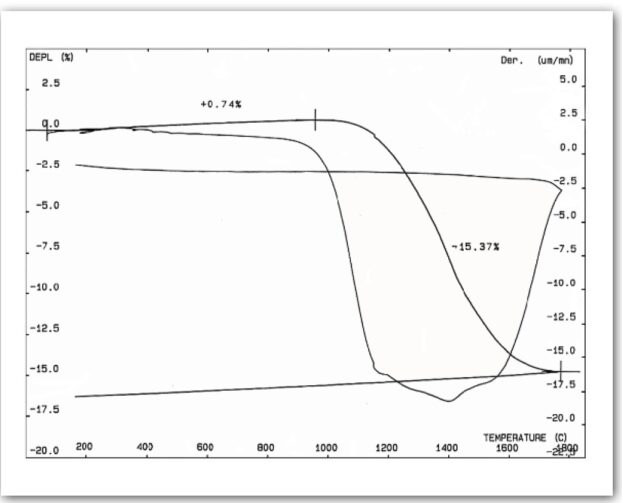
위 그래프에 대한 설명 : X축 – 온도 Y축 좌측 – 수축률 Y축 우측 – 수축속도
- 모델 THEMYS TMA를 이용하여 알루미나 시료의 소결 과정에서 발생하는 길이 변화(수축)와 수축 속도(shrinkage rate)를 동시에 측정한 결과입니다.
- 약 1100°C 이후부터 소결이 시작되면서 급격한 수축이 발생하며,
- 약 1300–1500°C 구간에서 수축 속도가 최대가 됩니다.
- 그래프에서 확인되는 **최종 수축량은 약 −15.37%**이며,
- 최대 수축 속도는 약 −17 μm/min 수준으로 나타납니다.
- 이러한 분석을 통해 세라믹 소결 공정에서 필요한 온도 프로그램과 수축 거동을 정밀하게 설계할 수 있습니다.
결과 및 결론
- 알루미나 시료를 5 K/min의 일정한 가열 속도로 가열할 경우,
- 소결로 인해 약 15%의 수축(shrinkage)이 발생하는 것이 관찰되었다.
- 이때 최대 수축 속도(maximum shrinking rate)는 약 60 μm/min으로 나타났다.
- 따라서 수축 속도를 20 μm/min 이하로 유지하기 위해서는,
- 가열 속도(K/min)를 자동으로 낮추어 제어할 필요가 있다.
- 이 방법의 가장 큰 장점은 단 한 번의 실험으로 일정한 수축 속도(constant shrinking rate)에서의 소결 온도 프로그램을 결정할 수 있다는 점이다.
- 이는 산업용 소결 공정에서 적용할 최적의 온도 프로파일을 설정하는 데 매우 유용한 정보를 제공한다.
탄화규소(SiC)의 소결:
모델 THEMYS – TMA 기능 사용

소개
- 소결(sintering)은 분말 상태의 재료를 가열하여 입자 간 결합을 증가시키고 하나의 고체 구조로 만드는 공정입니다.
- 이 공정은 세라믹 분말 및 분말 야금(powder metallurgy)에서 널리 사용됩니다.
- 예를 들어 탄화규소(SiC, Silicon Carbide)의 치밀한 세라믹을 제조하는 가장 일반적인 방법 중 하나는 무압 소결(pressureless sintering)입니다.
- SiC는 Si–C 결합이 강한 공유결합(covalent bond) 특성을 가지므로 원자 확산 속도(diffusion kinetics)가 매우 느립니다.
- 따라서 높은 치밀도(densification)를 얻기 위해서는 소결 촉진제(sintering enhancer)의 첨가가 필요합니다.
가장 널리 사용되는 조합은 다음과 같습니다.
- B + C (붕소 + 탄소)
- Al + C (알루미늄 + 탄소)
이러한 첨가제를 사용하면 이론 밀도(theoretical density)의 97% 이상의 소결 밀도를 얻을 수 있습니다.
실험 조건
시료는 미리 압축(precompacted)된 α-SiC 분말 큐브이며, 크기는 다음과 같습니다.
9 mm × 9 mm × 9 mm
실험 조건
- 분위기 가스: 아르곤(Ar)
- 적용 하중: 5 g
온도 프로그램은 다음과 같습니다.
- 20°C → 480°C : 가열 속도: 10 K/min 480°C에서 3시간 유지
- 480°C → 2200°C : 가열 속도: 15 K/min
- 2200°C → 실온 : 냉각 속도: 15 K/min
또한 실험 곡선은 동일한 실험 조건에서 시료 없이 수행한 blank 실험 결과를 이용하여 보정되었습니다.
결과 및 결론
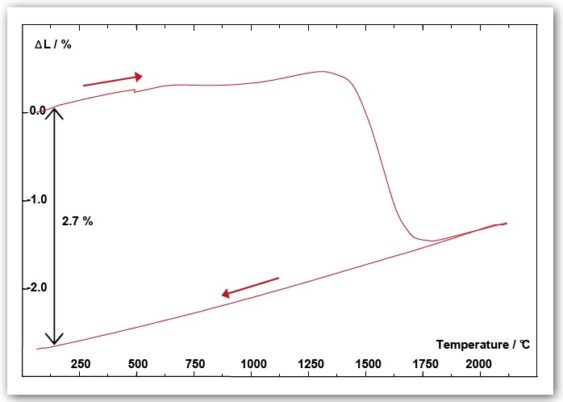
- 실험 결과에 따르면 실온에서 약 1310°C까지는 전체적으로 열팽창(expansion)이 나타납니다.
- 1310°C 이상에서는 수축(shrinkage)이 관찰되며, 이는 SiC 분말의 소결(sintering)이 시작되었음을 의미합니다.
- 이 소결 수축 과정은 약 1815°C에서 완료됩니다.
- 그 이후 1815°C 이상에서는 다시 SiC의 열팽창 현상이 나타납니다.
- 냉각 과정에서는 소결된 SiC의 열수축이 관찰되며,
- 실온까지 냉각된 후 **전체 소결 수축량은 약 2.7%**로 측정되었습니다.
지르코니아(SiC)의 열팽창 :
모델 THEMYS – TMA 기능 사용

소개
- 온도가 상승하면 모든 재료는 열팽창(thermal expansion)을 일으킵니다.
- 이로 인해 세라믹 부품이 가열될 때 치수 변화가 크게 발생할 수 있습니다.
- 열팽창계수(CTE, Coefficient of Thermal Expansion)는 온도 상승에 따라 재료가 얼마나 팽창하는지를 나타내는 열물성(thermophysical property)입니다.
- 이 값은 세라믹이 온도 변화에 대해 얼마나 치수 안정성(dimensional stability)을 유지할 수 있는지를 알려줍니다.
- 복잡한 구조에서 서로 접촉하는 부품들이 열팽창 특성이 서로 다를 경우, 내부 응력(internal stress)과 응력 집중(stress concentration)이 발생할 수 있습니다. 이러한 현상은 **조기 파손(premature failure)**의 원인이 될 수 있습니다.
- 따라서 열팽창계수(CTE)는 사용 중 온도 변화가 발생하는 모든 구조물의 품질과 신뢰성 확보에 매우 중요한 물성 값입니다.
실험 조건
- 시료: 지르코니아(Zirconia)
- 시료 길이: 19.90 mm
- 프로브: 알루미나 평면 프로브 (alumina flat-ended probe)
- 분위기 가스: 헬륨(He)
온도 프로그램
- 가열: 20°C → 1300°C : 가열 속도: 1.5 K/min
- 냉각: 1300°C → 20°C : 냉각 속도: 0.5 K/min
또한 동일한 실험 조건에서 시료 없이 blank 실험을 수행하여 측정 데이터를 보정하였습니다.
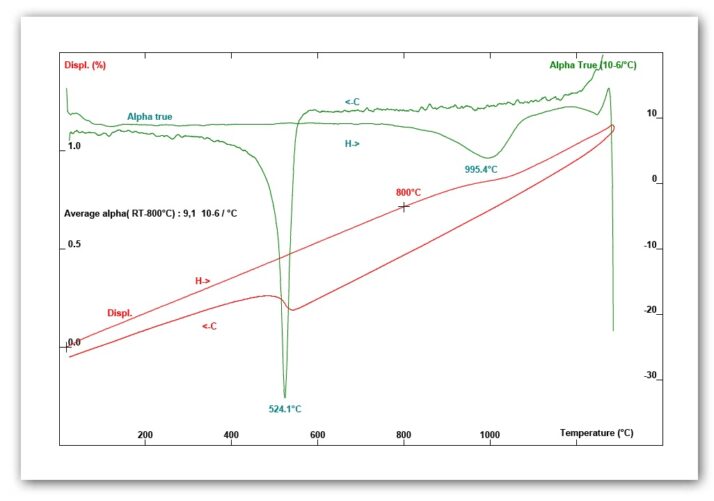
결과 및 결론
가열 과정에서 20°C ~ 800°C 구간의 평균 열팽창계수(CTE)는 9.1 × 10⁻⁶ /°C 로 측정되었습니다.
이 결과는 다음 요소에 대한 표준 보정(standard correction)을 적용한 후 얻어진 값입니다.
- 프로브(probe)의 열팽창
- 시료 홀더 튜브(sample holder tube)의 열팽창
- 장비의 측정 드리프트(instrumental drift)
이와 같은 열팽창 분석은 세라믹 부품의 온도 변화에 따른 치수 안정성 평가와 열응력 설계에 중요한 자료로 활용됩니다
고온에서 세라믹의 열용량 측정 :
모델 THEMYS ONE 사용

소개
- 세라믹 소재는 제조 공정이나 실제 사용 환경에서 고온에 노출되는 경우가 많습니다.
- 따라서 세라믹 전구체(precursor) 소재와 최종 세라믹의 열용량(Heat Capacity)을 정확하게 제어하는 것은 제조 공정의 안정성과 제품 성능을 보장하는 데 매우 중요합니다.
- 또한 열용량은 고온 환경에서의 열적 안정성 및 열노화(thermal ageing)에 대한 저항성을 평가하는 데 중요한 물성입니다.
이러한 열용량은 일반적으로 다음과 같은 방법으로 측정됩니다.
- DSC (Differential Scanning Calorimetry, 시차주사열량계)
- 열량계(calorimetry)
- 마이크로 열량계(microcalorimetry)
실험 조건
- 알루미나(Al₂O₃) 나노 분말 361 mg을 사용하여 실온에서 1400°C까지 비열(Cp)을 측정하였습니다.
- 측정은 연속 가열 방식(continuous heating method)으로 수행되었으며, 가열 속도는 20°C/min입니다.
- 비열 계산을 위해 사파이어(sapphire) 표준 시료를 이용한 보정(calibration)이 사용되었습니다.
실험 장비 및 온도 범위
- 장비: 모델 THEMYS ONE 열분석기
- 온도 범위: 30°C → 1,400°C
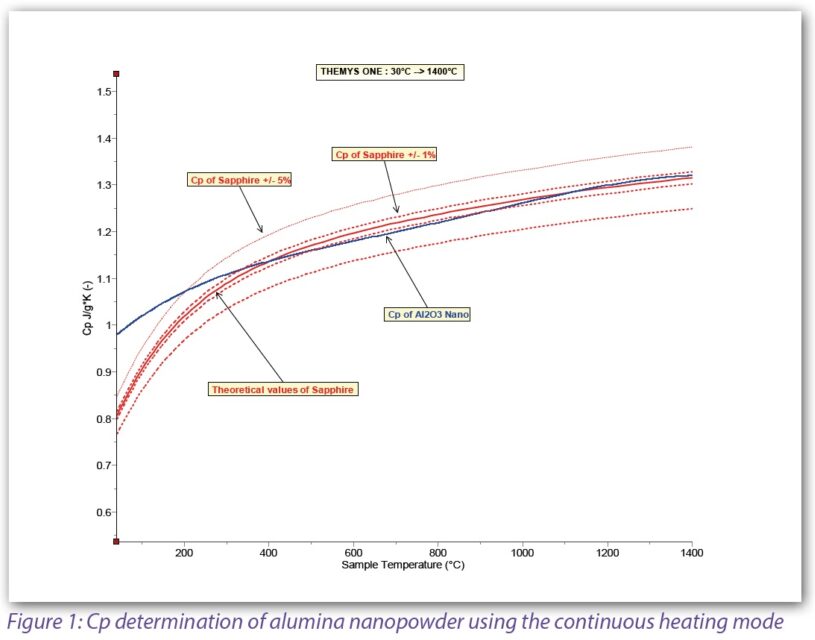
결과 및 결론
측정 결과 300°C 이상의 온도 구간에서 알루미나 나노 분말의 비열(Cp)은 1400°C까지 사파이어 기준값의 ±1% 범위 내에서 매우 높은 정확도를 유지하는 것으로 나타났습니다.
그래프에는 사파이어 비열 값을 기준으로 다음 두 가지 신뢰 구간(confidence interval)이 표시되어 있습니다.
- ±1% 범위
- ±5% 범위
알루미나 나노 분말의 측정 Cp 값은 ±1% 신뢰 구간 내에 위치하여 높은 측정 정확도를 보여주었습니다.
La0.65Mg0.15Ni0.20O3-d의 산소 화학양론 :
모델 THEMYS – TGA 사용

소개
- LaGaO₃ 기반 고체 전해질(solid electrolyte)과 이온–전자 혼합 전도체(mixed ionic–electronic conductor)는 고온 전기화학 장치에서 중요한 소재로 주목받고 있습니다.
- 특히 이러한 물질은 산소 화학양론(oxygen stoichiometry)과 금속 이온의 산화 상태(oxidation state)에 따라 전기적 및 화학적 특성이 크게 변합니다.
- 본 연구에서는 LaGa₀.₆₅Mg₀.₁₅Ni₀.₂₀O₃−δ 세라믹의 환원 거동(reduction kinetics)과 산소 비화학양론(oxygen non-stoichiometry)을 분석하기 위해 열중량 분석(TGA)을 이용하였습니다.
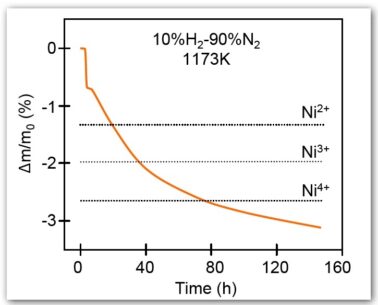
- 그림은 1173 K에서 10% H₂ – 90% N₂ 혼합 가스 분위기에서 수행한 환원 실험 결과의 예를 보여줍니다.
실험 조건
시료는 다음 조건에서 열중량 분석(TGA)을 수행하였습니다.
실험 과정
- 시료를 공기 분위기에서 2시간 유지
- 이후 아르곤(Ar) 분위기에서 1시간 유지
- 그 다음 10% H₂ – 90% N₂ 혼합 가스 분위기에서 144시간 환원
그래프의 점선(dashed line)은 다음 가정을 기반으로 계산된 이론적 질량 변화(theoretical weight change)를 나타냅니다.
- 갈륨 산화물(Ga₂O₃)의 휘발이 발생하지 않음
- 공기 중에서 니켈 이온이 Ni²⁺, Ni³⁺ 또는 Ni⁴⁺ 상태로 존재
산소 화학양론 측정 방법
LaGa₀.₆₅Mg₀.₁₅Ni₀.₂₀O₃−δ 세라믹의 산소 화학양론은
SETSYS TGA 열중량 분석기를 이용하여 측정하였습니다.
사용된 온도 프로그램
1.공기 분위기에서 3 K/min 가열
2.다음 온도에서 각각 2시간 평형 유지
- 1073 K
- 1123 K
- 1173 K
3.아르곤 가스로 1시간 퍼지(flushing)
4.이후 1173 K에서 10% H₂ – 90% N₂ 혼합 가스 분위기에서 환원
결과 및 결론
TG 데이터를 기반으로 계산한 공기 분위기에서의 산소 비화학양론(δ) 값은 다음과 같습니다.
| T (K) | δ | Average Ni oxidation state |
|---|---|---|
| 1173 | 0.080 | 2.95 |
| 1123 | 0.070 | 3.05 |
| 1073 | 0.062 | 3.13 |
분석 결과
- 1173 K에서 니켈 평균 산화수: +2.95
- 1073 K까지 냉각 시: +3.13까지 증가
이는 산화 분위기에서 LaGa₀.₆₅Mg₀.₁₅Ni₀.₂₀O₃−δ 격자 내에 Ni²⁺, Ni³⁺, Ni⁴⁺가 공존함을 의미합니다.
특히 Ni⁴⁺ 형성 가능성이 제시되었지만, 이는 아직 가설적 해석(hypothesis)으로 추가적인 실험적 검증이 필요합니다.
이는 산소 삽입(oxygen incorporation)에 의해 형성되는 전자 홀(electron hole)의 정확한 위치를 확인하기 위한 추가 연구가 필요하기 때문입니다.
산화물(Bi₂WO₆)의 생성열 :
DROP CALORIMETER인 모델 CALVET DC ALEXSYS 사용

소개
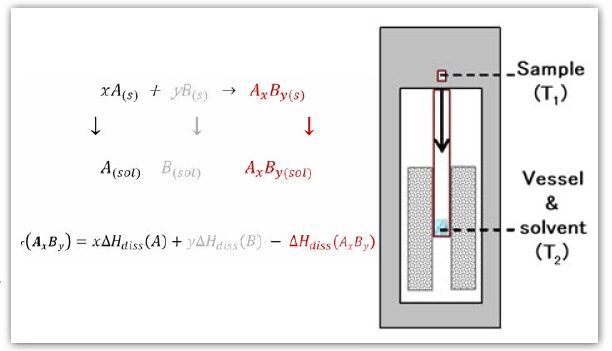
- Drop calorimetry(드롭 열량 측정)는 시료를 실온에서 고온의 열량계(calorimeter) 내부로 떨어뜨릴 때 발생하는 엔탈피 변화(enthalpy change)를 측정하는 방법입니다.
- 열량계 셀 내부에 용매(solvent)가 존재할 경우, 시료가 용매에 용해(dissolution)되면서 발생하는 용해열(heat of dissolution)도 측정되는 엔탈피 변화에 포함됩니다.
- Figure 1과 같이 일련의 용해 실험(dissolution tests)을 수행하면 물질의 생성 엔탈피(heat of formation)를 계산할 수 있습니다.
Step 1 선택된 동일한 용매에서 각 구성 성분의 용해열(heat of dissolution)을 측정
Step 2 Step 1에서 얻은 용해열 데이터를 결합하여 생성 엔탈피(heat of formation) 계산
실험 조건
장비
- CALVET DC ALEXSYS 열량계
시료
- Bi₂WO₆
- 전구체(precursors) → Bi₂O₃ WO₃
장비는 dual drop 기능을 갖추고 있으며, 시험 온도에서 시료를 투입할 수 있는 drop tube를 사용합니다.
Figure 1은 drop method를 이용한 생성 엔탈피 계산 방법을 보여줍니다.
여기서는 AxBy 형태의 화합물을 예로 설명하고 있지만, 이 방법은 다음과 같은 다양한 물질에 적용할 수 있습니다.
- 금속간 화합물 (intermetallics)
- 산화물 (oxides)
- 탄화물 (carbides)
- 기타 다양한 고온 화합물
결과 및 결론
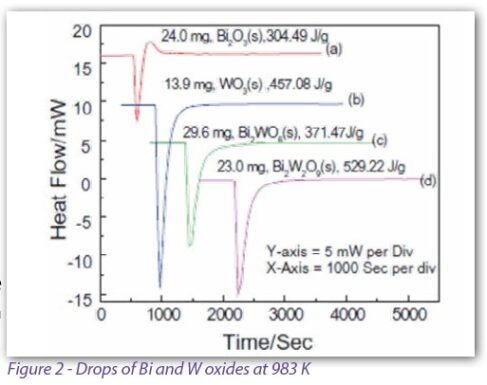
Figure 2에서 볼 수 있듯이 Heat Flow 신호에서 나타나는 피크를 적분(integration)하면 용해열(heat of dissolution)을 계산할 수 있습니다.
또한 Bi와 W가 각각 Bi₂O₃ 및 WO₃로 산화되는 반응의 산화열(heat of oxidation) 값은 문헌(literature)에서 확인할 수 있습니다.
실험 조건
- Drop solution method : 983 K
- 용매 : Na₂O + MoO₃ 용융 용액 (liquid solvent)
아래 Figure 3에 나타난 반응식을 이용하면 문헌 데이터와 실험 데이터를 결합하여 다음 반응의 *생성 엔탈피(enthalpy of formation)*를 계산할 수 있습니다.
Bi₂WO₆ 생성 반응 : Bi+W+O → Bi2WO6
Reaction scheme for the standard molar enthalpy of formation of Bi2WO6(s) (M(sln) = dilute solution of species M in 3 g liquid Na2O + MoO3, 3:4 M solvent maintained at 983 K).
ΔH°f298 = −ΔH1 + ΔH2 + ΔH3 + ΔH4 + ΔH5
| Reaction | ΔHi | ΔHi/(kJ · mol−1) | Reference |
|---|---|---|---|
| Bi2WO6(s,298 K) + (sln,983 K) = Bi2O3(sln,983 K) + WO3(sln,983 K) | ΔH1 | 118.93 ± 5.83 | This work |
| Bi2O3(s,298 K) + (sln,983 K) = Bi2O3(sln,983 K) | ΔH2 | 52.48 ± 4.82 | This work |
| WO3(s,298 K) + (sln,983 K) = WO3(sln,983 K) | ΔH3 | 43.07 ± 2.18 | This work |
| 2Bi(s,298 K) + 3/2O2(g,298 K) = Bi2O3(s,298 K) | ΔH4 | −574.00 ± 0.80 | Ref. [12] |
| W(s,298 K) + 3/2O2(g,298 K) = WO3(s,298 K) | ΔH5 | −828.60 ± 0.13 | Ref. [12] |
| 2Bi(s,298 K) + W(s,298 K) + 3O2(g,298 K) = Bi2WO6(s,298 K) | ΔH°f298 | −1426.0 ± 7.9 | This work |
Figure 3 – Reaction scheme for the standard molar enthalpy of formation of Bi2WO6(s), ΔH°f298 = −ΔH1 + ΔH2 + ΔH3 + ΔH4 + ΔH5
연관된 분석 장비 (Setaram 열분석기 라인업)
- STA (시차주사열량계 + 열중량 분석기) – 모델 THEMYS의 STA 기능
- TMA (열물성 분석기) – 모델 THEMYS 의 TMA 기능
- TGA (열중량 분석기) – 모델 THEMYS의 TGA 기능
- DSC (열용량 측정기) – 모델 THEMYS ONE의 3D DSC 기능
- Drop Calorimeter (낙하 열량계) – 모델 CALVET DC ALEXSYS
Setaram 상세 페이지 바로가기
- 세타람 전체 열분석기 라인업, 한미산업 사이트 보기
- DSC 일반버전 모델 세트라인 DSC, 한미산업 사이트 보기
- DSC 상위 버전 모델 칼벳 시리즈, 한미산업 사이트 보기
- DSC 상위 버전, DROP CALORIMETER, 모델 CALVET DC, 한미산업 사이트 보기
- DSC 상위 버전 모델 CALVET PRO, 세트람 사이트 보기
- TGA 일반 버전 모델 세트라인 (SETLINE TGA), 한미산업 사이트 보기
- TGA의 상위 버전, 모델 템이스 (=THEMYS), 한미산업 사이트 보기
한미산업
1999년 개업 이후, 지난 30여년간
- Tribology(마찰/마모/윤활/CMP 연마), 스크래치, 고온 경도계, 베어링 시험기 : 미유럽 일본의 유명 제조공급사인 BRUKER, PHOENIX Tribology, TABER, SHINTO Heidon, INNOWEP, AMTEC, TRICO사.
- 열분석기(DSC,TGA,STA,TMA), 고온진공로 : 스위스 KEP 그룹의 SETARAM SETSAFE, 미국 MRF사, 일본 ENEOS MATERIALS사의 수지 열경화 시험기 등
최첨단 장비들을 국내에 소개 및 판매 기술 지원하여 왔으며, 또한 이기술을 바탕으로 일부 품목 제조를 통하여 국산화에도 노력하여 왔습니다. 앞으로도 더욱 노력하여 국내 기술 발전에 이바지 하도록 하겠습니다.
상호: 한미산업
대표: 최동하
사업자등록번호: 219-02-82992
Address
서울특별시 송파구 송파대로 167, 문정역 테라타워 A동 6층 619호. (문정동 651) 우편번호 05855
찾아오시는 길
서울 지하철 8호선 문정역 3번 출구에서 도보 약 300m 거리에 위치해 있으며, 지하 보행 통로로도 연결되어 있어 우천 시에도 편리하게 방문하실 수 있습니다.
Tel. 02-3411-0173
Fax. 02-3411-0178
choi.dongha77@gmail.com
견적문의
한미산업. All rights reserved.